Elementos Químicos Ejemplos 2025: Metales, No Metales, Metaloides y Vida Cotidiana
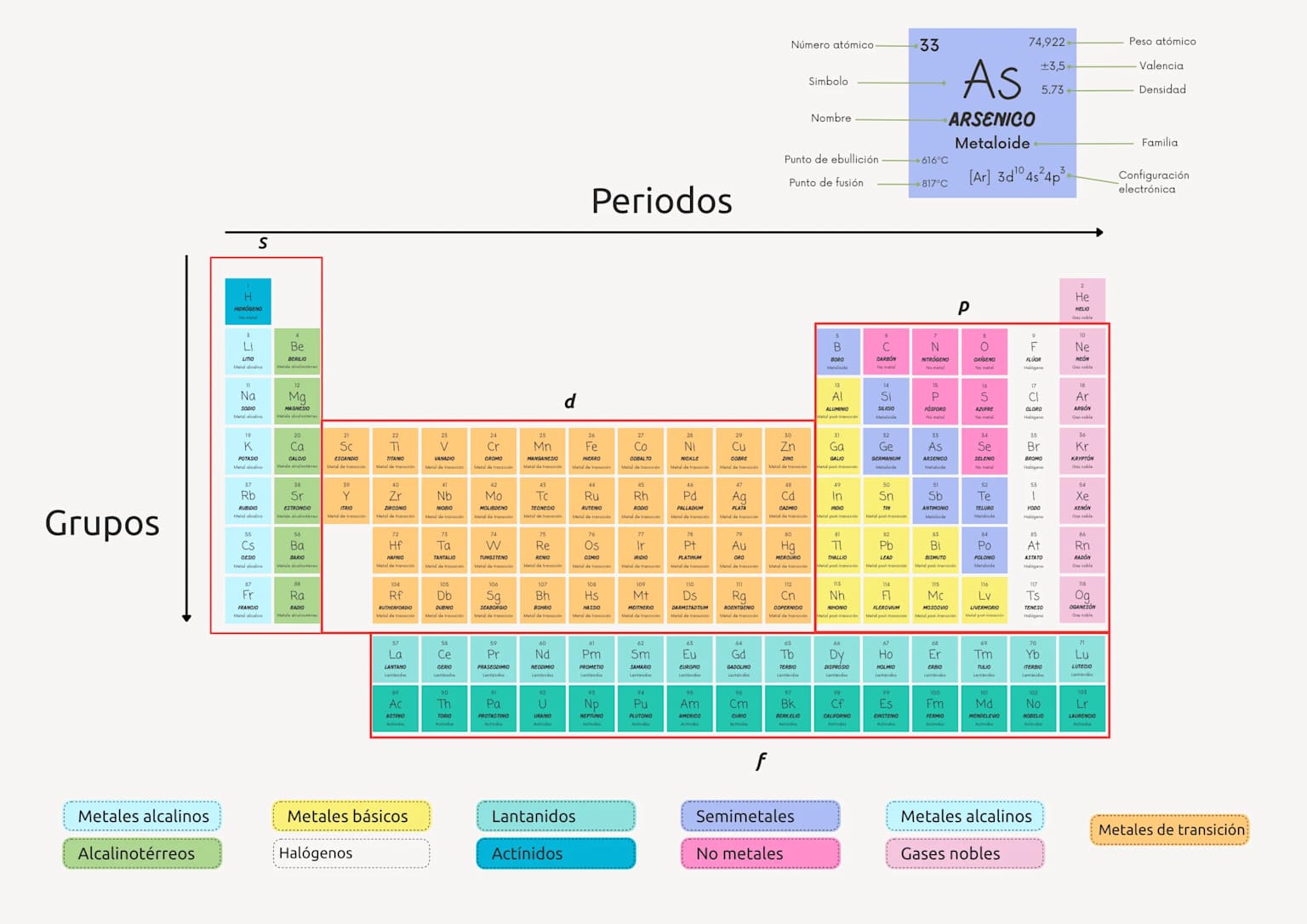
Los elementos químicos son las sustancias puras más simples que no pueden dividirse en sustancias más sencillas mediante reacciones químicas ordinarias. Actualmente se conocen 118 elementos registrados en la tabla periódica de la IUPAC: 94 de ellos ocurren de forma natural en la Tierra, y 24 son sintéticos, producidos en laboratorios. Cada elemento se define por su número atómico (la cantidad de protones en su núcleo), lo que determina sus propiedades físicas y químicas únicas. Esta guía incluye ejemplos concretos de todos los grupos de elementos químicos y sus aplicaciones reales en la vida cotidiana.
⚙️ Elementos Químicos Ejemplos: Metales
Los metales representan cerca del 73% de todos los elementos de la tabla periódica (86 de 118). Se caracterizan por ser excelentes conductores de electricidad y calor, presentar brillo metálico, ser maleables (se pueden laminar), dúctiles (se pueden estirar en hilos) y tener puntos de fusión generalmente altos.
Metales Alcalinos — Grupo 1
Son los metales más reactivos. Reaccionan violentamente con el agua. En la naturaleza siempre se encuentran combinados con otros elementos, nunca en estado libre.
- Sodio (Na, №11): Componente de la sal de mesa (NaCl), esencial para el funcionamiento del sistema nervioso y la regulación hídrica celular. El cuerpo humano contiene ~100 g de sodio.
- Potasio (K, №19): Abundante en plátanos, aguacates y papas. Vital para la función muscular, cardíaca y el balance electrolítico. Deficiencia causa calambres y arritmias.
- Litio (Li, №3): Utilizado en baterías de iones de litio (smartphones, autos eléctricos) y como estabilizador del estado de ánimo en psiquiatría (trastorno bipolar).
Metales Alcalinotérreos — Grupo 2
- Calcio (Ca, №20): Mineral más abundante del cuerpo humano (99% en huesos y dientes). Presente en lácteos, brócoli y sardinas. Esencial para la contracción muscular.
- Magnesio (Mg, №12): Cofactor de más de 300 enzimas. Presente en nueces, semillas y vegetales verdes. Fundamental para la síntesis de ATP.
- Bario (Ba, №56): Utilizado en sulfato de bario (BaSO₄) como contraste en radiografías gastrointestinales.
Metales de Transición — Grupos 3–12
El grupo más numeroso. Incluye los metales industriales y los metales preciosos. Son conocidos por sus múltiples estados de oxidación y colores característicos en solución.
- Hierro (Fe, №26): Base del acero (aleación Fe-C), componente de la hemoglobina que transporta oxígeno en la sangre. La deficiencia provoca anemia ferropénica.
- Cobre (Cu, №29): Mejor conductor eléctrico económico. Usado en cables eléctricos, tuberías y monedas. Esencial para la formación del colágeno.
- Zinc (Zn, №30): Fortalece el sistema inmune, cicatriza heridas. Utilizado en galvanización (protección anticorrosión del acero).
- Oro (Au, №79): Metal precioso casi inerte. Conductor perfecto sin oxidación. Usado en joyería, contactos electrónicos y nanotecnología médica.
🌿 Elementos Químicos Ejemplos: No Metales
Los no metales son 17 elementos que, a pesar de ser minoría en la tabla periódica, constituyen la base de toda la química orgánica y son indispensables para la vida. Son malos conductores del calor y la electricidad, tienden a ser frágiles en estado sólido y forman la mayor parte de la materia viva.
| Elemento | Símbolo | Nº Atómico | Estado (25°C) | Aplicaciones principales |
|---|---|---|---|---|
| Oxígeno | O | 8 | Gas | Respiración celular, combustión, medicina (terapia de O₂) |
| Carbono | C | 6 | Sólido | Base de todos los compuestos orgánicos, diamante, grafito, carbón activado |
| Nitrógeno | N | 7 | Gas | Fertilizantes (amoniaco), proteínas, atmósfera (78%), refrigeración criogénica |
| Fósforo | P | 15 | Sólido | ADN/ARN, ATP (energía celular), fertilizantes, cerillas |
| Azufre | S | 16 | Sólido | Ácido sulfúrico (industria), aminoácidos, pólvora, fungicidas |
| Hidrógeno | H | 1 | Gas | Agua (H₂O), combustible limpio, ácidos, síntesis orgánica |

Halógenos — Grupo 17
Los halógenos son los no metales más reactivos. Tienen 7 electrones de valencia y buscan atrapar uno más para completar su capa. Forman sales al reaccionar con metales.
- Cloro (Cl, №17): Desinfectante de agua potable y piscinas. Componente del cloruro de sodio (sal común) y del PVC. Altamente tóxico en estado gaseoso.
- Flúor (F, №9): El elemento más electronegativo de la tabla. Presente en pastas dentales (fluoruros) para prevención de caries. Es el no metal más reactivo conocido.
- Yodo (I, №53): Antiséptico clásico (tintura de yodo). Esencial para la síntesis de hormonas tiroideas (T3 y T4). Deficiencia causa bocio.
- Bromo (Br, №35): Utilizado en retardantes de llama, agroquímicos y fotografía analógica (bromuro de plata).
Gases Nobles — Grupo 18
Llamados también gases inertes o gases raros. Tienen configuración electrónica completa (8 electrones de valencia, excepto helio con 2), por lo que casi no reaccionan con otros elementos. Son todos incoloros, inodoros e insípidos a temperatura ambiente.
- Helio (He, №2): Globos y aeróstatos (densidad muy baja), refrigeración criogénica en resonancias magnéticas (MRI), mezclas de respiración para buzos.
- Neón (Ne, №10): Letreros luminosos "de neón" (emite luz naranja-roja al ionizarse), tubos de descarga, detectores de partículas.
- Argón (Ar, №18): Atmósfera inerte en soldadura TIG/MIG, relleno de bombillas incandescentes, ventanas con doble vidrio.
- Kriptón (Kr, №36) y Xenón (Xe, №54): Lámparas de flash fotográfico, lámparas de ion, anestésicos generales en medicina experimental.
💡 Elementos Químicos Ejemplos: Metaloides
Los metaloides (también llamados semimetales) son 7 elementos con propiedades intermedias entre metales y no metales. La característica más importante es que muchos son semiconductores: pueden conducir electricidad bajo ciertas condiciones de temperatura o voltaje, lo que los convierte en la base de la revolución tecnológica moderna.
- Silicio (Si, №14): El segundo elemento más abundante en la corteza terrestre (27.7%). Base de todos los microprocesadores, circuitos integrados, paneles solares y vidrio (SiO₂). Sin silicio no existirían las computadoras ni los smartphones modernos.
- Boro (B, №5): Componente del bórax (detergentes), fertilizantes para plantas, materiales cerámicos de alta resistencia, y el ácido bórico (antiséptico suave).
- Germanio (Ge, №32): Semiconductor de alta movilidad de electrones. Fibra óptica, detectores infrarrojos, diodos y transistores de alta frecuencia.
- Arsénico (As, №33): Dopante en semiconductores de arseniuro de galio (GaAs). Históricamente conocido como veneno; hoy también se usa en el tratamiento de ciertas leucemias (trióxido de arsénico).
🔬 Dato clave: El silicio (Si) es el fundamento de la industria tecnológica global. La región californiana donde nació la industria tecnológica se llama Silicon Valley precisamente por este elemento. Un chip moderno puede contener más de 100 mil millones de transistores de silicio.
🏠 Elementos Químicos Ejemplos en la Vida Cotidiana
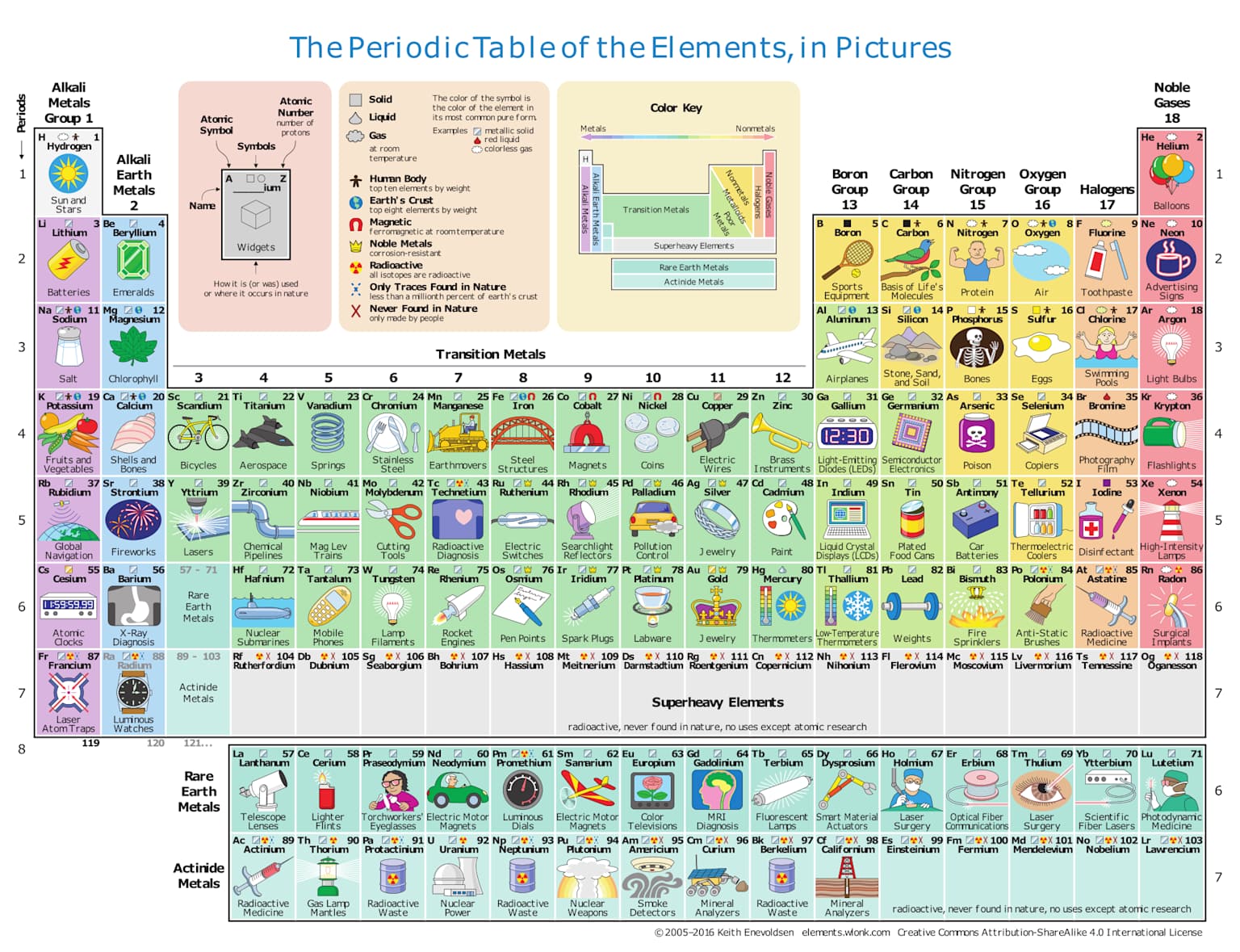
En los alimentos
- Calcio (Ca): Leche, queso, yogurt, sardinas, brócoli. Fortalece huesos y dientes, activa la coagulación sanguínea.
- Hierro (Fe): Carnes rojas, hígado, legumbres, espinacas. Componente de la hemoglobina (transporte de O₂). El 30% de la población mundial tiene deficiencia de hierro.
- Yodo (I): Sal yodada, pescados, mariscos. Síntesis de hormonas tiroideas T3 y T4 que regulan el metabolismo basal.
- Azufre (S): Proteínas con cisteína y metionina, ajo, cebolla, huevo. Importante para la estructura tridimensional de proteínas (puentes disulfuro).
- Fósforo (P): Carnes, legumbres, frutos secos. Base del ADN/ARN y del ATP (moneda energética celular). El 85% del fósforo corporal está en huesos y dientes.
En productos de higiene y medicina
- Aluminio (Al, №13): Desodorantes antitranspirantes (sales de aluminio bloquean poros), envases de alimentos, latas.
- Flúor (F): Pasta dental (fluoruro de sodio), agua fluorada, barnices dentales. Endurece el esmalte dental formando fluorapatita.
- Plata (Ag, №47): Apósitos antibacterianos (iones Ag⁺ destruyen bacterias), joyería, espejismos, esmalte dental.
- Zinc (Zn): Cremas solares (ZnO), pomadas cicatrizantes, suplementos para el sistema inmune.
- Cloro (Cl): Agua clorada para desinfección domiciliaria, blanqueador (hipoclorito de sodio), antisépticos quirúrgicos.
En tecnología y construcción
- Silicio (Si): Microprocesadores, chips de memoria, paneles fotovoltaicos, vidrio (silicato de sodio).
- Aluminio (Al): Aviones, estructuras arquitectónicas, marcos de ventanas, cables eléctricos aéreos (menor densidad que el cobre).
- Titanio (Ti, №22): Implantes médicos (biocompatible), estructuras aeroespaciales, pigmento blanco (TiO₂ en pinturas y cremas solares).
- Cobre (Cu): Cableado eléctrico (~60% del consumo de cobre), tuberías, circuitos impresos, aleaciones (bronce, latón).
🧬 Elementos Químicos en el Cuerpo Humano
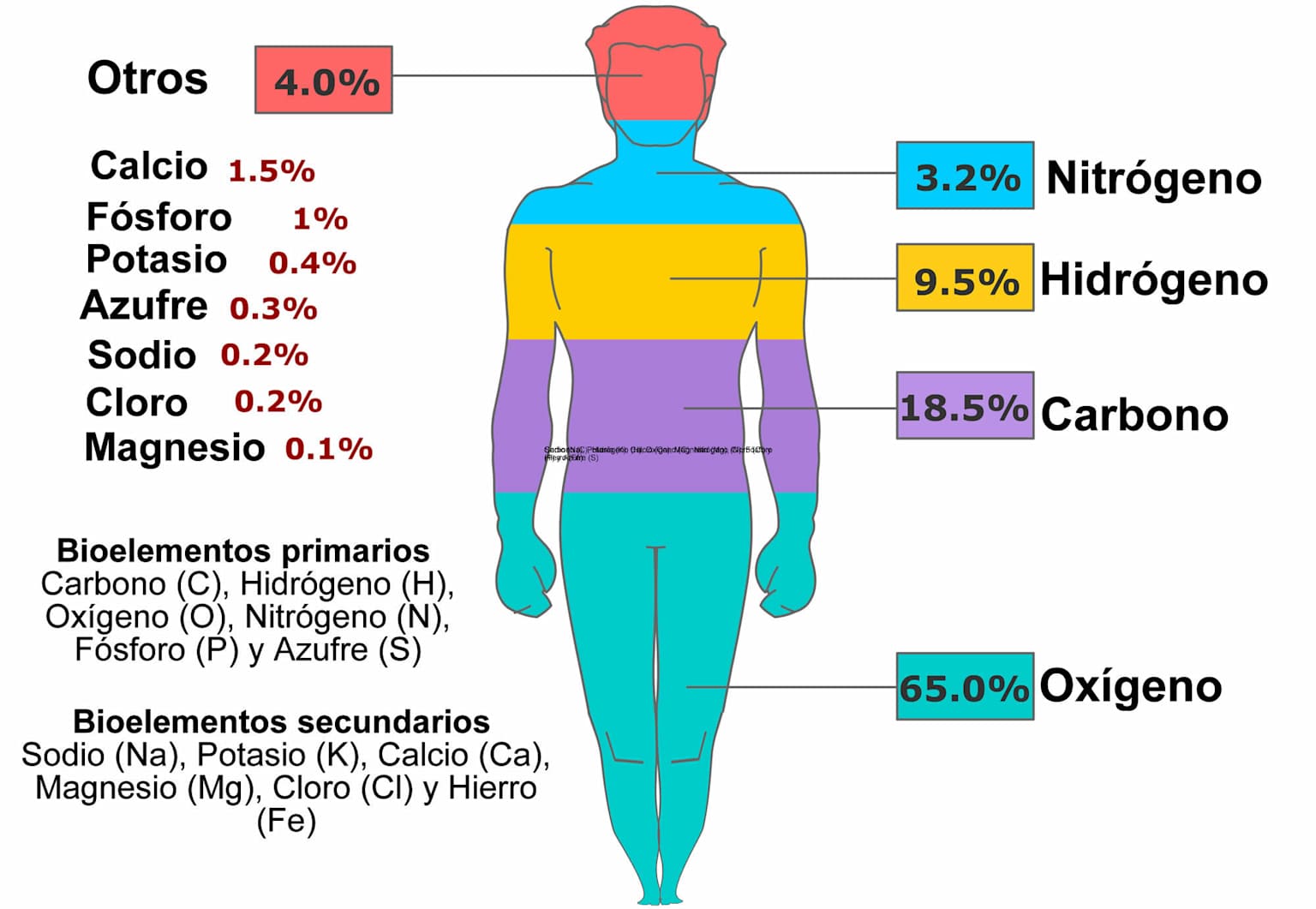
Bioelementos Primarios (96.2% del cuerpo)
Bioelementos Secundarios y Oligoelementos
- Calcio (Ca, 1.5%): Huesos, dientes, señalización celular, contracción muscular.
- Fósforo (P, 1%): ADN, ARN, ATP, huesos y dientes (como fosfato de calcio).
- Potasio (K, 0.4%): Principal catión intracelular. Regula el potencial de membrana de las neuronas.
- Azufre (S, 0.3%): Aminoácidos cisteína y metionina, puentes disulfuro en proteínas, queratina (cabello, uñas).
- Hierro (Fe, 0.004%): Hemoglobina (O₂), mioglobina (músculo), enzimas respiratorias. Solo 4g en un adulto, pero vitales.
- Zinc (Zn), Yodo (I), Selenio (Se), Manganeso (Mn): Oligoelementos en cantidades traza, pero cofactores de enzimas esenciales.
🌌 Abundancia de Elementos en el Universo
En el universo, la distribución de los elementos no es uniforme. Se originó durante el Big Bang (hidrógeno y helio) y posteriormente en el interior de las estrellas (nucleosíntesis estelar), que sintetizaron todos los demás elementos hasta el hierro. Los elementos más pesados se formaron en explosiones de supernovas.
🌟 Dato astronómico: Prácticamente todos los átomos que forman nuestro cuerpo — el carbono, oxígeno, nitrógeno y hierro — fueron sintetizados en el interior de estrellas que murieron hace miles de millones de años. Somos, literalmente, polvo de estrellas. El único elemento ligero que existió antes de las estrellas es el hidrógeno, formado 3 minutos después del Big Bang.
▶️ Video Educativo — Elementos Químicos en la Vida Cotidiana
Video educativo que explica los principales elementos químicos con ejemplos prácticos del día a día.
❓ Preguntas Frecuentes — Elementos Químicos Ejemplos
🔗 Recursos educativos recomendados
Información completa de los 118 elementos con propiedades y datos históricos.
Tabla periódica interactiva con datos detallados de cada elemento en español.
Tabla periódica oficial actualizada de la Unión Internacional de Química Pura y Aplicada.
Videos de laboratorio de la Universidad de Nottingham con experimentos de cada elemento.